El modelo atómico de Bohr, conocido también como modelo de Bohr-Rutherford, es un modelo clásico del átomo, es el primer modelo atómico en el cual se introduce la cuantización a partir de algunos postulados. Este modelo fue propuesto en el año de 1913 por Niels Bohr físico danés, dicho modelo explica que los electrones tienen órbitas alrededor del núcleo de manera estable y además que los átomos presentan espectros de emisión. Este modelo también se basa en algunas ideas del efecto fotoeléctrico, el cual fue dado por Albert Einstein en 1905.
Según este modelo que da Bohr (basado en el átomo de hidrógeno) se intenta realizar un modelo atómico que sea capaz de explicar la estabilidad de la materia y de los diferentes espectros de emisión y absorción que se observan en los gases. Además Bohr describe al átomo de hidrógeno con si fuese un protón dentro del núcleo, que gira alrededor del electrón.
Este modelo atómico también se basa en las ideas sobre cuantización de Max Planck, pero debido a lo simple de dicho modelo todavía es usado como la simplificación de la estructura de la materia.
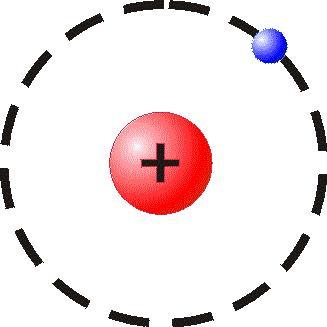
Entonces se entiende que según este modelo, los electrones se encuentran girando en órbitas circulares alrededor del núcleo, de tal manera que ocupan la órbita que tiene menos energía, o que se encuentre más cerca al núcleo.
Bohr interpretó que el momento angular que posee cada electrón se encuentra cuantizado y solamente puede variar en fracciones enteras de la constante de Planck, además dependiendo al número cuántico principal puede llegar a calcularse las distancias en las cuales se encuentra el núcleo en relación a cada una de las órbitas que están permitidas en el átomo de hidrógeno.
En resumen, el modelo atómico de Bohr propone un nuevo modelo atómico, el cual dice que los electrones pueden girar alrededor del núcleo pero en niveles que se encuentren bien definidos.
Lamentablemente el modelo atómico de Bohr debió ser abandonado, debido a que no podía explicar los espectros de los átomos más complejos, entonces el concepto de que los electrones se mueven alrededor del núcleo en órbitas definidas también fue una teoría descartada. Actualmente las teorias que se tienen sobre el átomo se encuentran basadas en la mecánica cuántica, concepto que el propio Bohr ayudó a desarrollar.
|
|
|
|
|
Modelos anteriores |
 |
|
|
|
|